「軽微」の検索結果
5件:1~5件目を表示
もしかして
-

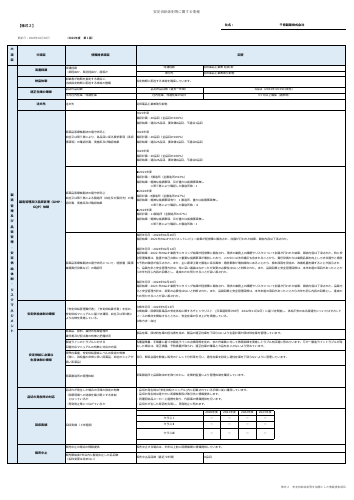
適切に情報提供すること。 備 考 アステラス製薬 2 変更の履歴 前回提出日: 令和 7 年 12 月 17 日 変更内容の概要: 1. 特定使用成績調査実施計画書、実施要綱、登録票及び調査票の更新(軽微な変更) (添付資 料) 変更理由: 1. 記載整備のため 1 医薬品リスク管理計画の概要 1.1 安全性検討事項 重要な特定されたリスク 眼内炎 重要な特定されたリスクとした理由: 一般に、硝子...
https://www.senju.co.jp/system/files/rmp_document/2026-03/IZV_202603_03_RMP.pdf -

: ①「品目の概要」の用法及び用量に「網膜静脈閉塞症に伴う黄斑浮腫」を追記した。 ②「品目の概要」の効能又は効果に「網膜静脈閉塞症に伴う黄斑浮腫」を追記した。 ③「添付文書」を「電子添文」に変更した(軽微変更) 。 変更理由: ①用法及び用量について、 「網膜静脈閉塞症に伴う黄斑浮腫」の承認事項一部変更承認申請を取 得したため。 ②効能又は効果について、 「網膜静脈閉塞症に伴う黄斑浮腫」の承認事項...
https://www.senju.co.jp/system/files/rmp_document/2023-10/RNB_202301_03_RMP.pdf -

承 認 条 件 医薬品リスク管理計画を策定の上、適切に実施すること。 備 考 2 変更の履歴 前回提出日:令和 2 年 4 月 6 日 変更内容の概要: ①医薬品リスク管理計画書を新様式に変更した(軽微変更) 。 ②「1.1 安全性検討事項」の「重要な特定されたリスク」に「角膜混濁」を追加した。 ③「添付文書」を「電子添文」に変更した(軽微変更) 。 変更理由: ①「医薬品リスク管理計画の策定及...
https://www.senju.co.jp/system/files/rmp_document/2024-07/ALM_202406_02_RMP.pdf -
全品目の82%)※他4品目については販売中止(製造停止)に伴い確認不要とした。 確認結果:適合17品目、要改善2品目、不適合0品目 ●2023年度 確認計画:10製造所(全製造所の33%) 確認結果:軽微な指摘事項、及び重大な指摘事項 無し ※第三者により確認した製造所数:1 ●2024年度 確認計画:12製造所(全製造所の30%) 確認結果:軽微な指摘事項有り 2 製造所、中程度な指摘...
https://www.senju.co.jp/about/rp/supply/form_2.pdf -

用成績調査」に関する情報を更新した。 ④「5.2 有効性に関する調査・試験の計画の一覧」における「抗菌活性の経年的推移に関する特定使 用成績調査(第 1 期、第 2 期) 」に関する情報を更新した(軽微変更) 。 ⑤医薬品リスク管理計画書を新様式に変更した(軽微変更) 。 ⑥「添付文書」を「電子添文」に変更した(軽微変更) 。 変更理由: ①~③小児(7 歳以上の結膜炎患者)を対象とする特定使用...
https://www.senju.co.jp/system/files/rmp_document/2023-09/AZM_202309_04_RMP.pdf






