「標」の検索結果
366件:16~20件目を表示
-

,文献・学会情報,外国措置報告,臨床試験等より報告される有害事象症例等の収 集・確認・分析に基づく安全対策の検討 追加の医薬品安全性監視活動 追加の医薬品安全性 監視活動の名称 節目となる症例数/ 目標症例数 節目となる 予定の時期 実施状況 報告書の 作成予定日 市販直後調査(適応症: 中心窩下脈絡膜新生血管 を伴う加齢黄斑変性) 該当せず 販売開始から 6 ヵ月後 終了 作成済 (2021 年...
https://www.senju.co.jp/system/files/rmp_document/2026-02/BEO_202601_02_RMP.pdf -

性の確認ならびに問題点の検出も行う。 【実施計画】 実施期間:調査開始から1年半とし、開始時期は発売1年目と4年目(計2回実施) 調査対象例数:各期 500例(合計1,000例を収集) 1期あたりの目標収集菌株数: ブドウ球菌属 150株 Staphylococcus aureus 50株 Staphylococcus epidermidis 40株 レンサ球菌属 15株 肺炎球菌 15株 コリネ...
https://www.senju.co.jp/system/files/rmp_document/2023-09/AZM_202309_04_RMP.pdf -

眼で重篤な有害事象と して眼内炎を発現した患者が海外第 2 相試験[OPH2002] (アバシンカプタド ペゴル 1 mg 群、表皮ブドウ球菌)において、1 例(25.0%)1 件報告された。本事象は標準治療 により回復し、治験担当医師により、本剤との関連性は否定され、投与手技との関連性 があると判断された。シャム群において報告はなかった。 医薬品安全性監視活動の内容及びその選択理由: 【内容】 ...
https://www.senju.co.jp/system/files/rmp_document/2026-03/IZV_202603_03_RMP.pdf -

ブロナック点眼液0.1%
度はいずれの測定時点においても定量下限 (50ng/mL) 未満であった1) 。 注) 本剤の承認された用法及び用量は 「通常、1 回 1 ∼ 2 滴、1 日 2 回点眼する。 」 である。 日本標準商品分類番号 承認番号 販売開始 22000AMX01226 2000年 7 月 871319 非ステロイド性抗炎症点眼剤 ブロナック点眼液0.1% 黄色澄明の無菌水性点眼剤 8.0∼8.6 販売...
https://www.senju.co.jp/system/files/product_other_file/2026-03/bronuck_202603_C4.pdf -
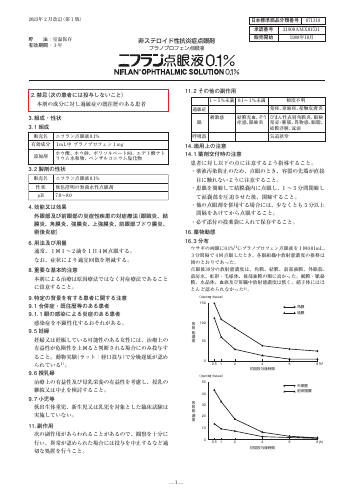
ニフラン点眼液0.1%
の放射能濃度は、角膜、結膜、前部強膜、外眼筋、 前房水、虹彩・毛様体、後部強膜の順に高かった。網膜・脈絡 膜、水晶体、血液及び肝臓中放射能濃度は低く、硝子体にはほ とんど認められなかった2) 。 日本標準商品分類番号 承認番号 販売開始 21900AMX01531 1988年10月 871319 非ステロイド性抗炎症点眼剤 プラノプロフェン点眼液 ニフラン点眼液0.1% 無色澄明の無菌水性点眼剤 ...
https://www.senju.co.jp/system/files/product_other_file/2025-12/niflan_202302_C1.pdf






