「18.9%」の検索結果
163件:131~135件目を表示
-

Dormolol_TE-C7_20240118
貯 法:室温保存 有効期間: 3 年 注) 注意─医師等の処方箋により使用すること 2. 禁忌 (次の患者には投与しないこと) 2. 1 本剤の成分に対し過敏症の既往歴のある患者 2. 2 気管支喘息又はその既往歴のある患者、気管支痙攣 又は重篤な慢性閉塞性肺疾患のある患者 [喘息発作の 誘発・増悪がみられるおそれがある。 ] [11.1.2参照] 2. 3 コントロール不十分な心不全、洞性徐脈
https://www.senju.co.jp/system/files/product_other_file/2024-03/dormolol_202302_C7.pdf -

ガチフロ点眼液0.3%
貯 法:室温保存 有効期間: 3 年 注) 注意─医師等の処方箋により使用すること 2. 禁忌 (次の患者には投与しないこと) 本剤の成分又はキノロン系抗菌剤に対し過敏症の 既往歴のある患者 ─ 1 ─ 3. 組成・性状 3. 1 組成 3. 2 製剤の性状 4. 効能又は効果 〈適応菌種〉 ガチフロキサシンに感性のブドウ球菌属、レンサ球 菌属、肺炎球菌、腸球菌属、モラクセラ (ブランハメ ラ)
https://www.senju.co.jp/system/files/product_other_file/2024-02/gatiflo_202405_C9.pdf -

ルミガン点眼液0.03%
貯 法:室温保存 有効期間: 3 年 2023年 2 月改訂 (第 1 版) 注) 注意─医師等の処方箋により使用すること ─ 1 ─ 3. 組成・性状 3. 1 組成 3. 2 製剤の性状 4. 効能又は効果 緑内障、高眼圧症 6. 用法及び用量 1 回 1 滴、 1 日 1 回点眼する。 7. 用法及び用量に関連する注意 頻回投与により眼圧下降作用が減弱する可能性がある ので、1 日 1 回
https://www.senju.co.jp/system/files/product_other_file/2023-01/Lumigan_202302_C1.pdf -
千寿製薬
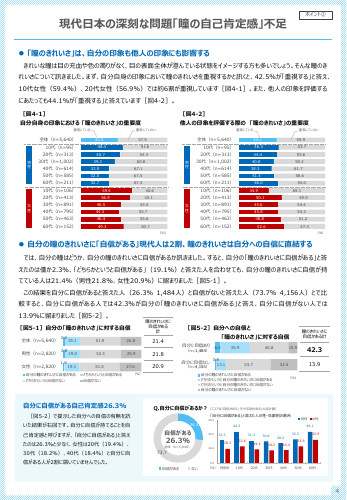
現代日本の深刻な問題「瞳の自己肯定感」不足 4 「瞳のきれいさ」は、自分の印象も他人の印象にも影響する きれいな瞳は目の充血や色の濁りがなく、目の表面全体が澄んでいる状態をイメージする方も多いでしょう。そんな瞳のき れいさについて訊きました。まず、自分自身の印象において瞳のきれいさを重視するかと訊くと、42.5%が「重視する」と答え、 10代女性(59.4%)、20代女性(56.9%)では約6
https://www.senju.co.jp/consumer/mytear/img/special/manga/point2.pdf -

医療関係者向製品情報(医療用医薬品) | 医療関係者のみなさま | 千寿製薬株式会社
製品一覧 関連情報 よくあるご質問 製品一覧PRODUCT 更新日: 2026年04月28日 50音で絞り込む ア カ サ タ ナ ハ マ ヤ ラ ワ 医療関係者向製品一覧をみる 製品名から探す後発医薬品情報(ジェネリック医薬品) 基本情報 製品写真・投薬袋イメージ 各種コード一覧 承認情報 規制区分・使用制限(有効期間)・貯法情報 封に関するお知らせ 製品名 製品写真 添付文書 インタビューフォ
https://www.senju.co.jp/medical/products/






