「×3」の検索結果
178件:81~85件目を表示
-

アジマイシン点眼液0.1%
貯 法:2 ∼ 8 ℃に保存 有効期間:3 年 注) 注意─医師等の処方箋により使用すること 2. 禁忌 (次の患者には投与しないこと) 本剤の成分に対し過敏症の既往歴のある患者 ─ 1 ─ 3. 組成・性状 3. 1 組成 3. 2 製剤の性状 4. 効能又は効果 〈適応菌種〉 アジスロマイシンに感性のブドウ球菌属、レンサ球 菌属、肺炎球菌、コリネバクテリウム属、インフル エンザ菌、アクネ菌
https://www.senju.co.jp/system/files/product_other_file/2022-11/AZM_C6_20221104.pdf -

ステロップ | 動物用医薬品・アニマルヘルス製品情報 | 飼い主・獣医師のみなさま | 千寿製薬株式会社
印刷する 動物用医薬品 犬用 抗炎症ステロイド点眼剤 ステロップⓇ イヌの結膜炎、角膜炎、眼瞼炎、ぶどう膜炎の治療に 色 剤形 容量 白色 乳濁点眼液 5mL 色 白色 剤形 乳濁点眼液 容量 5mL 飼い主さま向指導箋 添付文書 特性 イヌの眼科領域の抗炎症剤として、日本で初めてのステロイド性抗炎症点眼剤である 急性結膜炎およびぶどう膜炎などの、各種実験的眼炎症に抗炎症作用が認められている(イヌ
https://www.senju.co.jp/animal/veterinary/sterop.html -

ドライアイ治療剤 (TRPV1※拮抗薬) 2026年 4 月 6 日 統一商品コード HOT番号 薬価基準収載医薬品コード レセプト電算処理システム用コード 薬価基準収載日 薬 価 123-00498-5 1300260010101 2026年 3 月18日 123-00499-2 1300260010102 1319767Q1020 623002601 0.3% 5mL 1瓶 577.50円 包
https://www.senju.co.jp/system/files/news_file/2026-04/AVR_20260406.pdf -
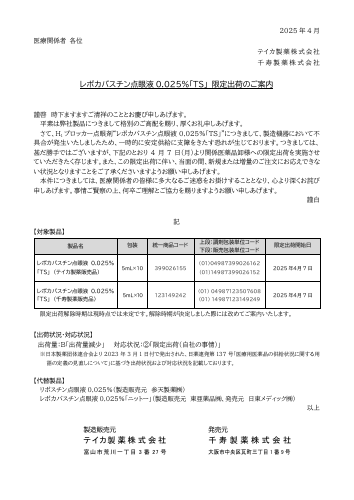
2025 年 4 月 医療関係者 各位 テイカ製 薬 株 式 会 社 千 寿 製 薬 株 式 会 社 レボカバスチン点眼液 0.025%「TS」 限定出荷のご案内 謹啓 時下ますますご清祥のこととお慶び申しあげます。 平素は弊社製品につきまして格別のご高配を賜り、厚くお礼申しあげます。 さて、H1 ブロッカー点眼剤“レボカバスチン点眼液 0.025%「TS」”につきまして、製造機器において不 具合
https://www.senju.co.jp/system/files/news_file/2025-04/LVC_20250407.pdf -

CYANOCOBALAMIN_TE_C3_20220425
貯 法:室温保存 有効期間: 3 年 2022年 7 月改訂 (第 1 版) ─ 1 ─ 3. 組成・性状 3. 1 組成 3. 2 製剤の性状 4. 効能又は効果 調節性眼精疲労における微動調節の改善 6. 用法及び用量 通常、 1 回 1 ∼ 2 滴を 1 日 3 ∼ 5 回点眼する。 なお、症状により適宜増減する。 9. 特定の背景を有する患者に関する注意 9. 5 妊婦 妊婦又は妊娠して
https://www.senju.co.jp/system/files/product_other_file/2022-06/CYN_C3_20220701.pdf






